исследование
Телемедицина в Германии во время пандемии COVID-19.

Стремясь сдержать последствия пандемии коронавирусного заболевания (COVID-19), системы здравоохранения во всем мире внедрили телемедицинские решения для преодоления кадровых, технических и инфраструктурных ограничений.
Однако масштабы текущего внедрения в различных медицинских учреждениях, принятие и восприятие пользователем, а также препятствующие технические и нормативные препятствия остаются неясными.
Статистические выбросы в лабораторных условиях

Статистическая идентификация и устранение выбросов — это тема, которая вызвала проблемы практически в каждой лаборатории. Существует множество причин для этого, в том числе ошибка измерения, выборки, неправильная запись или спецификация предположений о распределении. Когда первопричина неизвестна или не может быть легко идентифицирована, используются статистические методы для выявления потенциальных выбросов для восстановления.
Выбросы определяются как наблюдения, которые кажутся несовместимыми с остальной частью набора данных. Этот набор данных может иметь более одного выброса, хотя в лабораторных условиях он встречается редко. Прежде чем приступать к статистическому анализу, данные должны быть проверены на предмет допущений.
Графические методы могут использоваться для визуального принятия допущений, таких как нормальность и отсутствие выбросов. Некоторые методы включают в себя блочную диаграмму, гистограмму и график нормальной вероятности. Другие графические методы могут быть использованы по мере необходимости или целесообразно.
Проблема заключается в том, что выбросы могут искажать и уменьшать информацию, содержащуюся в источнике данных или механизме генерации. В лабораторных условиях наличие выбросов подорвет эффективность и точность любого полученного результата. Возможные выбросы не обязательно являются плохими или ошибочными; они просто не отражают ожидаемый результат метода. В некоторых ситуациях выброс может нести важную информацию, и поэтому ее следует определить для дальнейшего изучения. Данные, которые изначально определены как выбросы, могут быть показаны как часть ожидаемого распределения после сбора дополнительных параметров. Часто они содержат ценную информацию о расследуемом процессе или процессе сбора и записи данных.
Прежде чем рассматривать возможное исключение этих точек из данных, следует попытаться понять, почему они появились и вероятно ли подобные значения можно будет увидеть в будущем. Другими словами, находятся ли эти значения в пределах точности и достоверности метода?
Тест на выбросы
Как только наблюдение идентифицируется с помощью графического или визуального осмотра в качестве потенциального выброса, следует начать анализ первопричины, чтобы определить, может ли быть найдена назначаемая причина для ложного результата. Если невозможно определить основную причину, и повторное тестирование может быть оправдано, потенциальный выброс должен быть записан для будущей оценки, когда появится больше данных. Удаление точек данных на основе статистического анализа без определенной причины недостаточно. Статистическая значимость не подразумевает причинно-следственную связь. Надежные или не параметрические методы являются альтернативными для анализа.
Некоторые общие тесты на выбросы — это обобщенный экстремальный сдвиг (GESD) и Q-тест Диксона. На практике количество выбросов в выборке должно быть небольшим. Если в наборе данных много выбросов, это перестает быть проблемой обнаружения, и требуются другие подходы.
Соблюдение правил в регулируемых лабораториях.
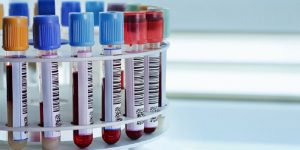
Прежде чем аналитические результаты могут быть получены, лаборатории требуется подходящий калиброванный инструмент, обученный аналитик, одобренный / утвержденный метод, соответствующие справочные материалы, стандартная рабочая процедура, чтобы гарантировать, что инструмент используется последовательным и воспроизводимым образом. И образцы для тестирования , если рассматривать их с точки зрения «принципов соблюдения», эти пункты необходимы для поддержки / защиты достоверности результатов анализа и могут рассматриваться как практически независимые от отрасли, в которой используется инструмент. На высоком уровне «жизненный цикл соответствия», за которым следует лаборатория для внедрения нового инструмента — от начальных инвестиций в бизнес до обоснования, управления и утверждения полученных аналитических результатов — должен:
- Быть основанным на здравом деловом и научном обосновании
- Рассмотрим материалы для тестирования
- Определите, как будет использоваться инструмент
- Документирование результатов расчета и отчетности
- Поддержите решения, по которым будут использованы результаты.
Различные регулируемые отрасли по-разному подходят к вопросу соответствия лаборатории и могут использовать термины уникальным образом. Для лабораторий в разных частях одной и той же организации нет ничего необычного в том, чтобы использовать индивидуальные подходы к соблюдению правил или разные термины. Эти различия могут ограничивать обмен информацией и передовым опытом. Часто жаргон, используемый в определенном секторе или отрасли, может усложнить понимание для внешних лабораторий. Различия могут стать очевидными только тогда, когда организации решают согласовать подходы к соблюдению или когда аналитический метод переносится из одной лаборатории в другую. Термин «калибровка» может сам по себе иметь очень специфическое значение и определение (например, аккредитованная в соответствии со стандартом ISO 17025 служба калибровки) или он может иметь более общее значение. Метролог будет работать с определением «калибровки», которое отличается от определения аналитика, руководителя лаборатории или аудитора. Когда выражение «калибровка» используется в фармацевтической испытательной лаборатории, оно может иметь ряд возможных значений в зависимости от действующей системы управления качеством и коммуникационных предпочтений человека. Выражения «Калибровка, аттестация, валидация и проверка» являются примерами терминов соответствия, которые иногда используются скорее как метки, которые представляют вид деятельности, а не как очень точное определение, используемое в стандарте ИСО. В интересах ясности, хотя Кодекс федеральных правил (CFR) 2 часто дает общее руководство по системам и политикам, которые лаборатория должна иметь для обеспечения соответствия, она не обязательно определяет точные детали или процессы, которым должна следовать, чтобы соответствовать требованиям. Для фармацевтических лабораторий один из способов интерпретации этой позиции заключается в том, что CFR обеспечивает надлежащую производственную практику (GMP), и организация должна сделать ее актуальной. Как правило, система менеджмента качества обеспечивает базовую структуру соответствия, которая удовлетворяет общим нормативным требованиям, таким как CFR, а также определенным процедурам и СОП, чтобы удовлетворять существенным деталям того, как лаборатории остаются совместимыми.
Одним из потенциальных рисков в лабораториях является то, что персонал может быть хорошо обучен процедурам, но плохо понимает основополагающие принципы качества. Это может означать, что изменения, необходимые для реализации улучшений, могут быть трудны для внедрения в лабораториях, где внимание и обучение сосредоточены на следующих процедурах, а не на применении основополагающих принципов соответствия. Кроме того, когда требуется думать «вне процедур» (например, когда возникает отклонение качества), может возрасти риск того, что отклонение не будет хорошо исследовано / задокументировано и что возможные последствия могут быть не полностью оценены.
Часть неопределенности в отношении соответствия инструментов связана с отсутствием четких указаний. Например, в отсутствие строгих руководств по соблюдению нормативных требований многие крупные фармацевтические организации приняли принципы надлежащей практики автоматизированного производства (GAMP).
К сожалению, принципы валидации процесса, определенные в работе были интерпретированы и по-разному применены к лабораторным приборам фармацевтическими компаниями, производителями приборов и консультантами. Во многих лабораториях это привело к плохому пониманию того, что требуется для внедрения новых инструментов, что может задержать возврат инвестиций в результате рисков соответствия.
Фундаментальная важность соответствия лаборатории означает, что она должна быть ключевым стратегическим приоритетом для управления. Тем не менее, ежедневное давление на работу и приоритеты бизнеса нередко ограничивают стратегическое мышление соответствия скорее реагированием, а не проактивностью; это приводит к тем случаям, когда «готовность к проверке» является не стратегическим приоритетом, а работой, выполненной непосредственно перед аудитом.
